di Gruppi Italiani Astrofisica Nucleare Teorica e Sperimentale
L’origine di idrogeno ed elio, così come quella del litio, risale alla prima mezz’ora di vita dell'Universo, mentre questo si stava velocemente raffreddando successivamente al Big Bang. Gli altri elementi sono stati prodotti da stelle formatesi nel corso dei successivi miliardi di anni. In questo schema generale fanno eccezione solo il berillio ed il boro, principalmente prodotti attraverso processi di spallazione (ovvero di “rottura” di un nucleo più pesante in nuclei più leggeri) provocati dai raggi cosmici.
Le stelle sono in grado di produrre tutti gli elementi chimici ad esclusione dell’idrogeno la cui creazione richiede le condizioni fisiche estreme del Big Bang. Prima di entrare nel vivo della discussione, è necessario introdurre il concetto di plasma perché è lo stato in cui si trova la materia nel gas stellare. Quando un atomo si trova a temperature superiori al milione di gradi (condizione tipica degli interni stellari), gli elettroni, che in condizioni terrestri orbitano attorno al proprio nucleo, possono viaggiare liberamente senza essere intrappolati dai relativi nuclei: coabitano quindi ioni positivi (i nuclei) e ioni negativi (gli elettroni). In questo plasma avvengono le reazioni nucleari che producono energia. Per esempio all’interno del nucleo del Sole (una stella molto rappresentativa della popolazione di stelle nel cosmo) si produce energia tramite la conversione di 4 atomi di idrogeno in 1 atomo di elio.
L’energia prodotta dalle reazioni nucleari crea una pressione che sostiene la stella, come si vede in figura, evitando che imploda su se stessa per l’enorme forza gravitazionale dovuta alla sua massa. Il primo ad immaginare che nelle stelle l’energia necessaria a controbilanciare la forza di gravità provenisse dalla combustione termonucleare dell’idrogeno fu Sir Arthur Eddington nel 1920. Anche se al tempo non poteva sapere che in questo processo di combustione si producono altri due tipi di particelle nucleari, i positroni e i neutrini, la sua intuizione resta un caposaldo della fisica stellare.
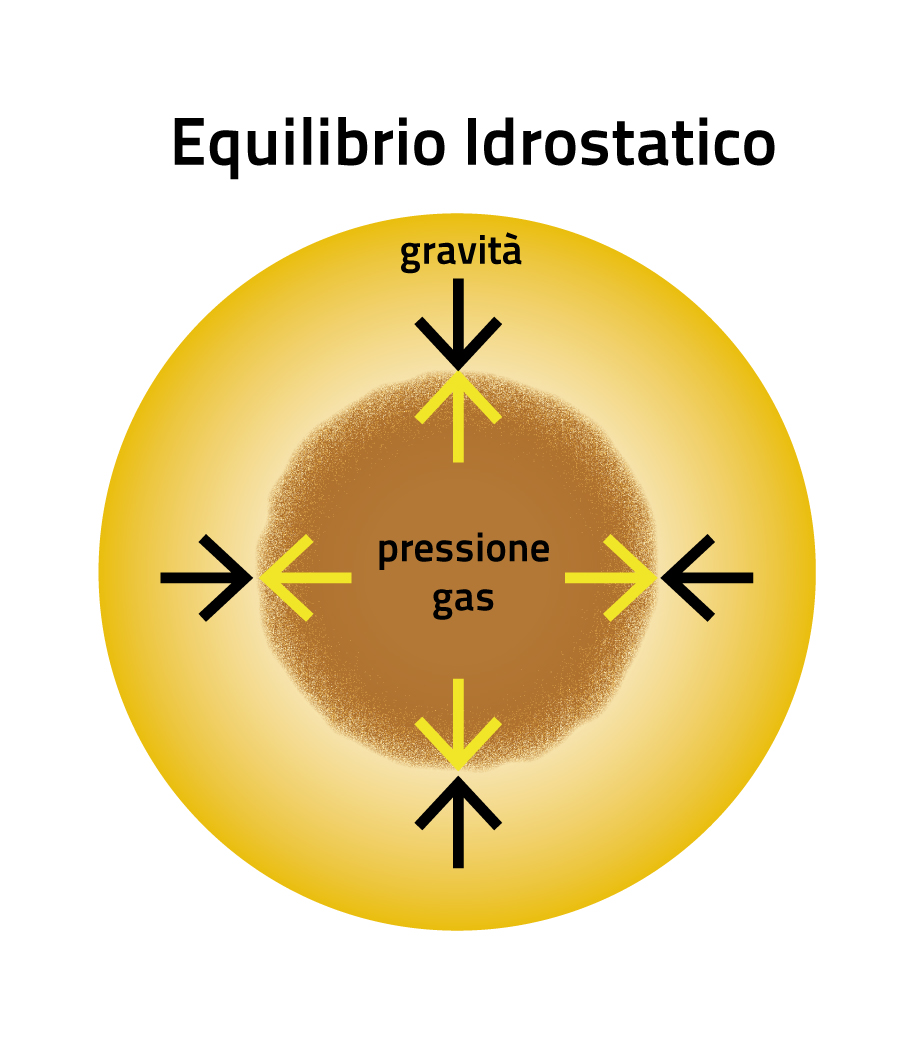
Immagine estratta da http://www.oa-abruzzo.inaf.it/CRISTALLO/periodictable2019_ita.html
Nel Sole, il processo di trasformazione di H in He avviene attraverso tre fasi successive. Durante la prima, due nuclei di idrogeno si fondono, producendo un nucleo di deuterio (formato da 1 protone ed 1 neutrone). Durante questo processo uno dei due protoni si è dunque trasformato in un neutrone. È così avvenuto quello che si definisce un decadimento ß inverso, ossia un processo che vede come protagonista principale la forza nucleare debole. A sua volta, il deuterio cattura un protone e forma un nucleo di 3He (2 protoni ed 1 neutrone). Infine, due nuclei di 3He si fondono, producendo un nucleo di 4He (costituito da 2 protoni e 2 neutroni) e rilasciando due protoni. Dal bilancio delle masse delle particelle partecipanti, vediamo che 4 protoni vanno a formare un nucleo di elio, la cui massa, però, risulta essere minore della somma delle masse dei 4 nuclei di idrogeno.
Dov’è finita la massa mancante? Ce lo spiega Einstein, o meglio la sua nota equazione E=mc2. In poche parole, la massa si è tramutata in energia. Se applichiamo questa formula al Sole, vediamo che da ben 4,6 miliardi di anni il Sole produce energia con una potenza di 4 miliardi di miliardi di miliardi di watt, e di conseguenza ogni secondo la sua massa diminuisce di 4,26 milioni di tonnellate!
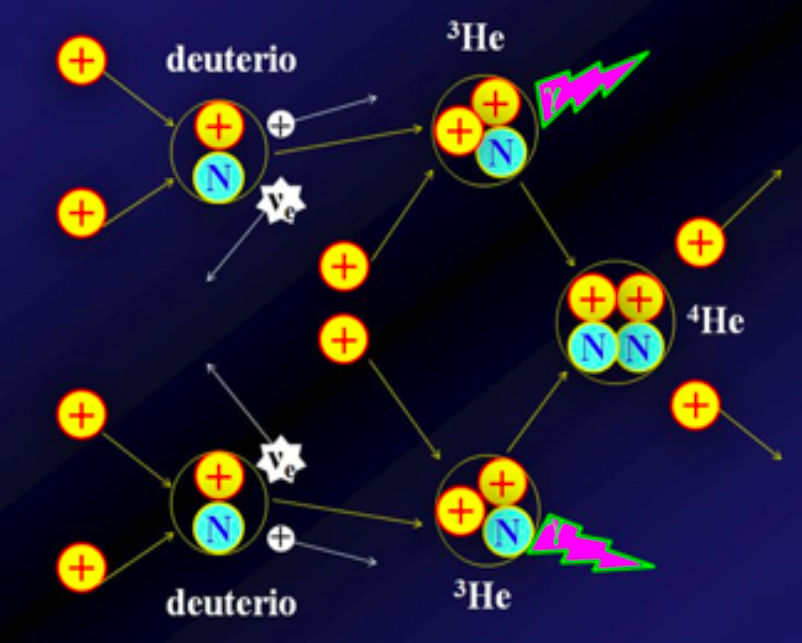
Immagine estratta da http://www.oa-abruzzo.inaf.it/CRISTALLO/periodictable2019_ita.html
Vale la pena notare che l’elio è continuamente prodotto tramite questa catena di reazioni nucleari nelle stelle, tuttavia ad oggi la frazione di elio prodotta con questo meccanismo è inferiore al 20% dell’elio prodotto nel Big Bang.

